Antonio Jesús Bellón Alcántara. Doctor Especialista en Digestivo y Medicina Interna

La reactivación de la hepatitis B asociada con inmunosupresores y terapias biológicas está surgiendo como una causa importante de morbilidad y mortalidad en pacientes con exposición actual o previa al virus de la hepatitis B (VHB). La población en riesgo de reactivación del VHB incluye a aquellos que están infectados actualmente con el VHB o que han estado expuestos anteriormente a dicho virus. Dado que la terapia curativa y erradicativa para el VHB no está disponible actualmente, existe un gran reservorio de individuos en riesgo de reactivación del VHB en la población general. La reactivación del VHB con sus posibles consecuencias es particularmente preocupante cuando estas personas están expuestas a quimioterapia contra el cáncer, a terapias inmunosupresoras o biológicas para el tratamiento de afecciones reumatológicas, tumores malignos, enfermedades inflamatorias del intestino, afecciones dermatológicas o trasplantes de órganos sólidos o de médula ósea.
Durante décadas hemos asumido que los pacientes que se recuperan clínica y analíticamente de un episodio de hepatitis aguda por el VHB, realmente aclaran el virus del organismo. Sin embargo, con el paso de los años, la investigación básica ha demostrado que la erradicación completa del VHB raramente ocurre (incluso en los pacientes positivos para anti-HBs, que son los anticuerpos neutralizantes del VHB que confieren inmunidad).
Y ésto es así porque el VHB posee un genoma constituido por DNA relajado circular (DNArc) que es abierto pero se transforma en DNA circular covalentemente cerrado (DNAccc), o superenrollado, en el núcleo de las células que infecta, permaneciendo en ellas indefinidamente ya que se integra en el genoma de los hepatocitos; esta infección latente conserva la respuesta de las células T que mantiene al virus bajo control (Yotsuyanagi 1998, Guner 2011, Gerlich 2013, Zhong 2014). El DNAccc es resistente a todos los antivirales conocidos hasta la fecha y solo puede ser eliminado por apoptosis de las células infectadas.
Todos estos descubrimientos de la investigación básica son muy importantes y de ellos podemos inferir varias deducciones:
1.-Cualquier persona que haya sufrido una infección por el VHB, aunque esté “curada” clínica y analíticamente, puede albergar una infección oculta por el VHB en la que no se detecta el marcador de infección HBsAg -antígeno de superficie del VHB-, pero sí presenta su genoma (DNA-VHB) en muestras de suero y/o tejido hepático. Esta situación se conoce internacionalmente con las siglas inglesas OBI (Occult HBV Infection).
2.-En consecuencia, no debemos hablar de Hepatitis B aguda curada, sino resuelta.
3.- El tratamiento de la hepatitis crónica B en la actualidad es subóptimo, ya que consigue el control de la enfermedad pero no la erradicación del VHB.
4.-Según la OMS, existen más de 360 millones de portadores crónicos del VHB a nivel mundial, pero esta estimación, por razones obvias, no incluye a aquellos que presentan una infección oculta.
5.- La inmunosupresión puede llevar a la reactivación del VHB, por ejemplo, después del trasplante de órganos o durante la quimioterapia (Di Bisceglie, 2014). Durante el tratamiento inmunosupresor puede ocurrir una reactivación de una infección asintomática o inactiva por VHB en un 20-50% de los pacientes (Lok, 2009). Las reactivaciones pueden ocurrir en portadores del HBsAg, pero también en pacientes negativos para el HBsAg pero positivos para el anti-HBc IgG.
Estudios previos han mostrado que la reactivación del VHB por terapias anti-cáncer ocurre en el 41-53% de los pacientes HBsAg positivos (Lau, 2003) y en el 8-18% de los HBsAg negativos, anti-HBc IgG positivos (Huang, 2013).
La tasa de reactivación del VHB por terapias antirreumáticas se ha descrito en el 12,3% de los pacientes HBsAg positivos (Lee, 2013) y en el 1,7% de los HBsAg negativos, anti-HBc IgG positivos (Mori, 2015).
6.-Sabemos que los anti-HBs son anticuerpos neutralizantes del VHB que confieren inmunidad frente al mismo; sin embargo, aún no se ha establecido su papel en el cribado antes de la terapia inmunosupresora. La presencia de anti-HBs no evita la reactivación del VHB, pero su pérdida puede ser un factor predictivo de la reactivación del mismo (Kanaan, 2012, Onozawa 2005, Hammond 2009).
7.-Las reactivaciones del VHB se caracterizan por un incremento de la replicación del virus, seguido de un aumento de la inflamación hepática durante el proceso de reconstitución immune, lo que conduce a daño hepático e, incluso, insuficiencia hepática en algunos pacientes (Feld 2010, Roche 2011).
8.-Es necesario prevenir la reactivación del VHB antes de iniciar un tratamiento inmunosupresor o quimioterápico; para ello, se debe realizar un cribado del VHB en todos los pacientes que van a ser sometidos a estos tratamientos, mediante los siguientes marcadores: HBsAg, anti-HBs cuantificado y anti-HBc IgG. En los pacientes que presenten positividad a alguno de estos marcadores, debe determinarse también el DNA-VHB cuantificado y valorar si precisan profilaxis de la reactivación o tratamiento. En ambos casos, los fármacos a emplear deben ser potentes y de alta barrera genética frente a las resistencias, tales como Entecavir o Tenofovir.
Aquellos pacientes que resulten negativos para HBsAg, anti-HBs cuantificado y anti-HBc IgG, deben vacunarse contra el VHB.
La reactivación del VHB refleja la pérdida del control inmunitario del virus en pacientes HBsAg positivos, o HBsAg negativos con anti-HBc IgG positivos que están recibiendo terapia inmunosupresora para una afección médica concomitante.
La American Association for the study of liver diseases (AASLD) define la reactivación del VHB según los siguientes criterios (Fig. 1):

Figura 1 (Tomado de: Terrault NA et al.-Hepatology, Vol 67, nº 4, 2018)
Hasta ahora nos hemos referido preferentemente a los factores virológicos, pero existe otro aspecto muy importante a tener en cuenta, que es el concerniente al tipo y grado de inmunosupresión que pretendemos administrar al paciente. Así, el número de potenciales dianas terapéuticas en el tratamiento de las enfermedades neoplásicas y autoinmunitarias se ha incrementado de forma notable en los últimos años, lo que ha dado lugar a la aparición de nuevos y potentes fármacos que han venido a enriquecer el arsenal terapéutico de estas enfermedades; no obstante, estos nuevos medicamentos interactúan potencialmente con los mecanismos responsables del control inmunológico de la replicación del VHB, lo que provoca en muchas ocasiones una reactivación del mismo.
A este respecto, se han establecido tres categorías de fármacos según el riesgo que conllevan de reactivación del VHB y que detallamos en la figura 2.
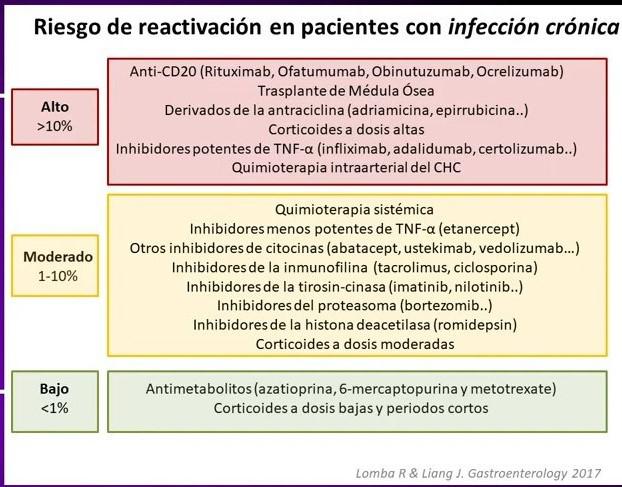
(Tomado de: Loomba R, Liang J.-Gastroenterology. 2017 May; 152(6): 1297-1309)
Por último, los factores del huésped incluyen el sexo masculino, la edad avanzada, la presencia de cirrosis y los diferentes tipos de enfermedades que necesitan inmunosupresión, por ejemplo, los linfomas.
En lo que se refiere a la duración de la profilaxis anti-reactivación, la European Association for the Study of the Liver (EASL) recomienda que ésta se mantenga al menos 12 meses (18 meses para regímenes con Rituximab) tras el cese del tratamiento inmunosupresor y solo debe interrumpirse si la enfermedad subyacente está en remisión.
Durante el seguimiento deben realizarse controles con pruebas de función hepática y DNA-VHB cuantificado cada 3-6 meses hasta 12 meses tras la interrupción de la profilaxis (hasta dos años después de la última dosis para regímenes con Rituximab).
Por último, en la figura 3 detallamos un algoritmo para el manejo de la reactivación de la hepatitis B.
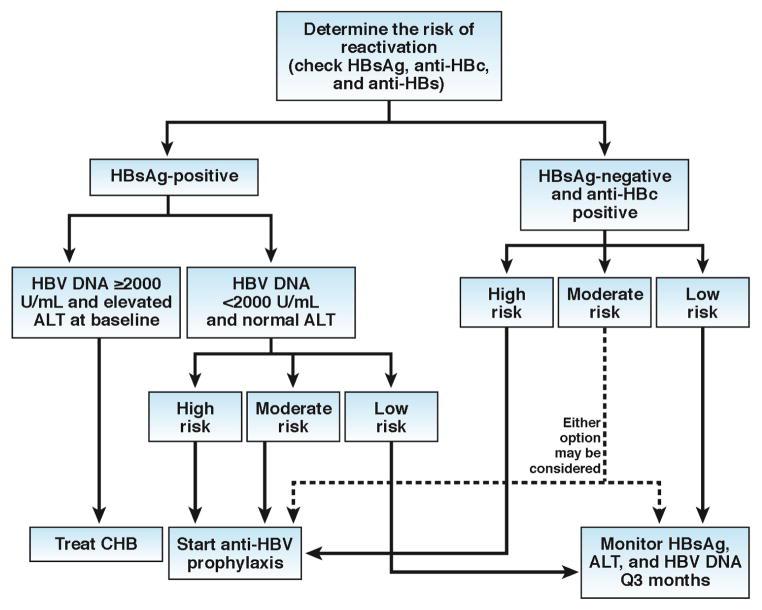
Figura 3: Algoritmo para el manejo de la reactivación de la hepatitis B.
(Tomado de: Loomba R, Liang J.-Gastroenterology. 2017 May; 152(6): 1297-1309)
Como puede apreciarse en el algoritmo, si el DNA-VHB es ≥ 2000 U/mL y las transaminasas están elevadas por encima de la basal, se debe realizar tratamiento de la hepatitis crónica B (CHB). Como ya hemos comentado anteriormente, los fármacos a emplear, tanto para profilaxis como para tratamiento, deben ser potentes y de alta barrera genética frente a las resistencias, como Entecavir o Tenofovir.