Antonio Jesús Bellón Alcántara. Doctor y Académico Correspondiente de Medicina. Especialista en Medicina Interna y Aparato Digestivo. Miembro de la Asociación Española para el Estudio del Hígado.
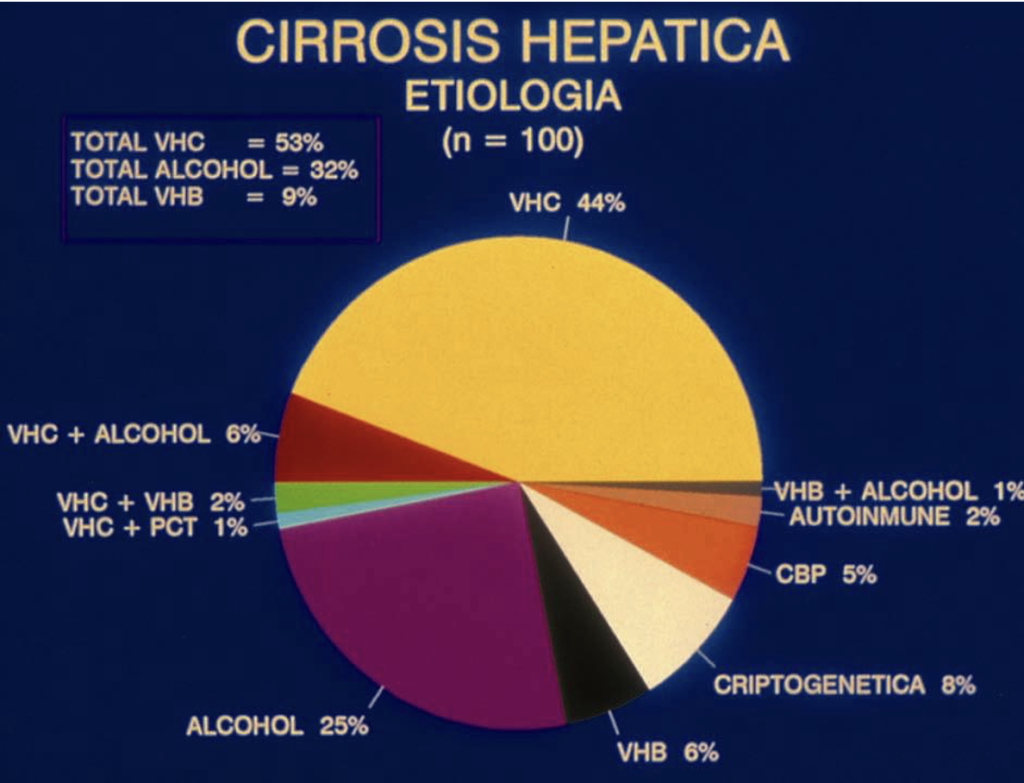
El virus de la hepatitis C (VHC), identificado en 1989 (Houghton et al.EurPatentAppl 88,310,922.5,1988), ha sido hasta fechas muy recientes la primera causa de hepatitis crónica, cirrosis y cáncer de hígado en España. En la figura 1 podemos observar las diversas etiologías de la cirrosis hepática en nuestro medio, según un estudio prospectivo que realizamos sobre 100 pacientes cirróticos (Bellón,RealAcadMedCir Cádiz,29-32,2000).
Según la memoria general de resultados del Registro Español de Trasplante Hepático de 2021, en el periodo 1984-2021 se realizaron 28.071 trasplantes hepáticos, de los cuales 5.698 fueron debidos a cirrosis por VHC, suponiendo la segunda causa por detrás de la cirrosis alcohólica.
Se trata, por tanto, de un problema de salud pública de primera magnitud.
El virus de la hepatitis C (VHC) está constituido por un genoma de RNA monocatenario y no posee transcriptasa inversa, por lo que no puede integrarse en el genoma de las células que infecta, a diferencia del virus de la hepatitis B (VHB), que sí puede hacerlo; por lo tanto, la erradicación del VHC es perfectamente posible. En consecuencia, el tratamiento de la hepatopatía crónica por VHC debe tener como finalidad conseguir la erradicación del virus, traducida en la práctica clínica por la desaparición definitiva y permanente del RNA-VHC en el suero del paciente.
La historia natural de la hepatitis C crónica sigue un curso paralelo al acúmulo de fibra colágena en el hígado, determinando el riesgo de progresar hasta la cirrosis, de presentar hipertensión portal, descompensación clínica y la probabilidad de desarrollar carcinoma hepatocelular (CHC). Por tanto, en el estudio de los pacientes con hepatitis C es fundamental la evaluación precisa del grado de fibrosis. El desarrollo de fibrosis es un proceso dinámico, no lineal y variable de un paciente a otro, por lo que su evaluación requiere valoraciones repetidas a lo largo del tiempo.
Si bien la biopsia hepática se sigue considerando como el patrón de referencia para la evaluación del estadio de fibrosis, en el momento actual existen numerosos procedimientos capaces de estimar de forma adecuada el grado de fibrosis hepática. Una clasificación inicial permite diferenciar procedimientos invasivos (biopsia hepática, medición del gradiente de presión venosa hepática y endoscopia alta) y no invasivos (evaluación clínica, marcadores séricos, métodos radiológicos clásicos y métodos elastográficos). Todos ellos presentan una aceptable precisión diagnóstica, si bien ninguno de ellos está exento de inconvenientes.
La elastografía determina la rigidez del hígado, la cual es proporcional al grado de fibrosis y de hipertensión portal. Existen dos tipos de elastografía: de compresión y por onda de cizallamiento. El método elastográfico que más ha evolucionado es la elastografía por onda de cizallamiento, con tres técnicas diferentes de medición: “Transient Elastography” o elastografía transitoria (ET), “Point Shear-Wave Speed Measurent” y “Shear-Wave Speed Imaging”. Los resultados se expresan en kilopascales (kPa) en un rango amplio y con una mínima variabilidad intra e interobservador.
Según la Guía de la AEEH/SEIMC de manejo de la Hepatitis C de marzo 2017, se debe evaluar el estadio de fibrosis en todos los pacientes con hepatitis crónica por el VHC, utilizando métodos no invasivos con elevados valores predictivos para excluir o identificar fibrosis avanzada, debiéndose reservar la biopsia hepática para la evaluación de pacientes con enfermedades concomitantes o con valores discordantes de los métodos no invasivos. Dado que la elastografía cumple los criterios antedichos, éste es el principal medio diagnóstico utilizado en la práctica clínica para evaluar la fibrosis hepática en los pacientes con hepatopatía crónica por VHC.
En cuanto a la terapia, en 1989 se autorizó la comercialización del Interferón alfa-2a (Roferón®) para el tratamiento de la hepatopatía crónica por VHC. Fue precisamente Hoofnagle el pionero en el tratamiento de dicha afección con este fármaco, el cual comenzó a ensayar incluso varios años antes de la identificación del VHC, cuando la enfermedad aún se denominaba Hepatitis No A No B (Hoofnagle et al.-NEJM;315:1575-1578.1986).
Nuestra experiencia en el tratamiento de la hepatopatía crónica por VHC se remonta a 1992. En aquellos años, la eficacia terapéutica se definía exclusivamente según la respuesta de las transaminasas; así, cuando las ALT se normalizaban, se hablaba de respuesta completa y si las ALT, sin llegar a normalizarse, descendían por debajo del 50% del nivel basal se denominaba respuesta parcial. Ambos tipos de respuesta se consideraban exitosas en los primeros estudios.
En el año 1999 se comercializó en España un nuevo fármaco contra el VHC, la Ribavirina (Rebetol®) el cual, administrado por vía oral, potenciaba la acción terapéutica del Interferón. El tratamiento combinado de Ribavirina más Interferón alfa hacía posible la erradicación virológica sostenida (respuesta virológica sostenida) en aproximadamente el 40% de los pacientes tratados.
En el 2000, un nuevo medicamento vino a enriquecer el arsenal terapéutico contra el VHC; se trataba del Peginterferón alfa-2b (Pegintron®), un derivado del Interferón alfa-2b recombinante conjugado covalentemente con monometoxipolietilenglicol, el cual aumenta significativamente las propiedades farmacocinéticas y la actividad antivírica clínica. La pegilación del Interferón alfa-2b permitió prolongar su actividad al retrasar significativamente su aclaramiento renal, aumentando así su semivida plasmática de aproximadamente 4 horas a 40, y permitiendo de esta forma una única administración a la semana. En nuestra experiencia, la respuesta virológica sostenida (RVS) (RNA-VHC indetectable en el suero 6 meses después de finalizado el tratamiento) se consiguió en el 50% de la muestra global (incluidos pacientes cirróticos) y en el 62,5% de los pacientes no tratados previamente (naive patients); en ninguno de los pacientes que consiguieron la RVS reapareció el RNA-VHC en el suero tras un periodo de observación de varios años (respuesta virológica permanente) (Bellón, Monog Schering-Plough, 2005;77-93).
Por todas estas razones el tratamiento de Interferón pegilado + Ribavirina sustituyó al de Interferón estándar + Ribavirina.
Durante once años, del 2000 al 2011, los clínicos dispusimos, por tanto, de un tratamiento eficaz pero con muchos efectos adversos, algunos graves, que requerían un hábil manejo de los fármacos por parte del médico y una gran resiliencia por parte de los enfermos.
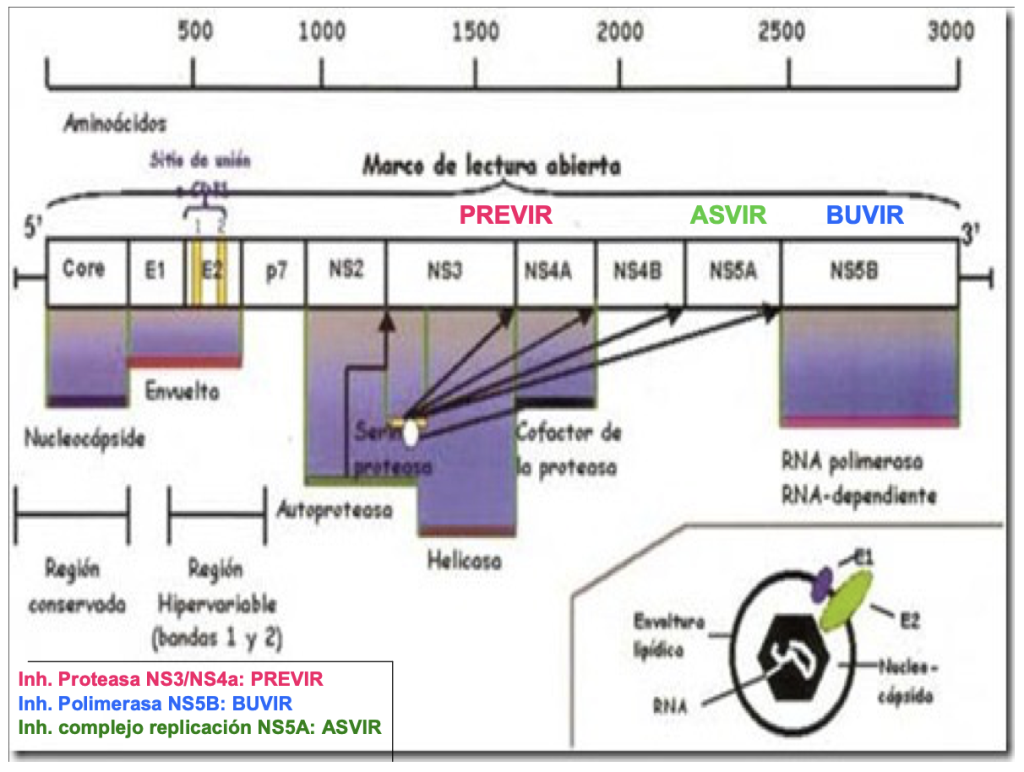
En el año 2011 aparecen en el mercado español los inhibidores de la proteasa del VHC de primera generación, Boceprevir (Victrelis®) y Telaprevir (Incivo®). Estos son los primeros antivirales directos contra el VHC, puesto que actuaban inhibiendo la proteasa de serina NS3/NS4A, una enzima esencial para la replicación del virus (Figura 2).
Aunque estos nuevos fármacos mejoraban la respuesta virológica sostenida, sin embargo, no podían ser usados en monoterapia sino asociados al Peginterferón alfa y Ribavirina, con lo cual aumentaban significativamente los efectos adversos, incluso con complicaciones fatales, lo que llevó a establecer un Plan de minimización de riesgos. Además, solo eran eficaces en el genotipo 1 del VHC.
A partir del año 2014 comienzan a aparecer en el mercado español los antivirales directos de segunda generación, tales como Sofosbuvir (Sovaldi®), Simeprevir (Olysio®), Daclatasvir (Daklinza®), Sofosbuvir/Ledipasvir (Harvoni®), Ombitasvir/Paritaprevir potenciado con ritonavir(Viekirax®), Dasabuvir (Exviera®), Elbasvir/Grazoprevir (Zepatier®), Sofosbuvir/Velpatasvir (Epclusa®), Sofosbuvir/Velpatasvir/Voxilaprevir (Vosevi®), Glecaprevir/Pibrentasvir (Maviret®).
En la tabla 1 se recogen los antivirales de acción directa (AAD) disponibles en la actualidad.
| Diana terapéutica | Fármacos |
| Inhibidores proteasa NS3/NS4A (-previres) | Simeprevir (SMV), Paritaprevir potenciado con Ritonavir (PTVr), Grazoprevir (GZV), Glecaprevir, Voxilaprevir (VOX) |
| Inhibidores proteína NS5A (-asvires) | Ledipasvir (LDV), Elbasvir (EBV), Daclatasvir (DCV), Velpatasvir (VEL), Ombitasvir (OBV), Pibrentasvir |
| Inhibidores polimerasa NS5B (-buvires) | Sofosbuvir (SOF), Dasabuvir (DSV) |
La aparición de estos nuevos antivirales marcó un hito en el tratamiento de la hepatitis C por dos razones fundamentales: en primer lugar, por las mejores expectativas de curación que despertaban, tanto en los pacientes como en los médicos y, en segundo término, por el coste tan elevado de los mismos, sin precedentes en este tipo de fármacos. Piénsese que Sofosbuvir (Sovaldi®), el primer antiviral directo de segunda generación que recibió la autorización para su comercialización en España en 2014, salió al mercado en EEUU con un precio de 84.000 dólares por tratamiento completo. Dado que la duración habitual del tratamiento era de 12 semanas (84 días), Sovaldi® fue conocido como “la pastilla de los 1.000 dólares”.
Este precio tan elevado unido al hecho de que la hepatopatía crónica C supone en España un problema muy importante de salud pública, determinó que el Pleno del Consejo Interterritorial del Sistema Nacional de Salud en su sesión del 14 de enero de 2015 adoptara la decisión por unanimidad de elaborar un Plan Estratégico para el abordaje de la Hepatitis C en el Sistema Nacional de Salud.
Sin duda, el aspecto más controvertido a nivel social de las conclusiones de dicho Plan Estratégico, fue el hecho de que priorizara la instauración del tratamiento antiviral para determinados grupos de pacientes, especialmente aquellos con una fibrosis hepática avanzada (F2-F4); en los pacientes con fibrosis hepática leve (F0-F1) el tratamiento se podía diferir y considerar su indicación individualmente.
Este hecho, como era previsible, provocó un gran malestar entre estos últimos pacientes, los cuales se sintieron excluidos y sin esperanza de ser tratados a corto plazo.
Afortunadamente, sólo dos años después, el Consejo Interterritorial del Sistema Nacional de Salud de fecha 21/06/2017 acordó la ampliación del tratamiento de la hepatitis C con antivirales de segunda generación a todos los pacientes, independientemente del estadio de la enfermedad. Esta decisión se tomó en base a la gran eficacia de dichos antivirales y a la significativa bajada de precios de los mismos.
Estos grandes avances terapéuticos y una adecuada planificación logística en nuestro país, han permitido que la infección crónica por VHC sea en la actualidad una enfermedad fácilmente curable en sólo doce semanas, siéndolo en nuestra experiencia en el 100% de los pacientes.
Por otra parte, la hepatitis C es una enfermedad bien definida, frecuente, con una historia natural conocida, con un periodo de latencia prolongado, en la que las intervenciones de prevención primaria son coste-efectivas y cumple los criterios que establece la Comisión de Salud Pública del Ministerio de Sanidad en relación a los programas de cribado y de diagnóstico precoz. La estrategia de cribado y diagnóstico precoz puede aplicarse a toda la población o a determinadas poblaciones de riesgo; hasta la fecha se ha promovido el diagnóstico precoz en poblaciones prioritarias, en las que la prevalencia de infección por el VHC es alta. No obstante, estudios recientes de modelización en poblaciones de prevalencia baja, como la española, en la era de los antivirales de acción directa (AAD) de segunda generación, muestran que el cribado poblacional universal es más coste-efectivo que el realizado por grupos de riesgo u otra estrategia.
En resumen, podemos afirmar con satisfacción que estamos asistiendo en la actualidad al ocaso de la Hepatitis C. Resulta sorprendente que se haya conseguido un tratamiento antiviral de tan alta eficacia capaz de erradicar el VHC, negativizando de forma permanente el RNA-VHC sérico y, sin embargo, aún no se haya elaborado una vacuna que genere protección frente a todos los genotipos del virus. Esperemos que en un futuro no muy lejano podamos disponer de la misma y que pueda ser aplicada a escala mundial.